Dettagli
- Definizione e caratteristiche
- Localizzazione
- Varianti
- Epidemiologia
- Eziologia e patogenesi
- Storia e caratteristiche cliniche
- Diagnosi
- Stadiazione
- Gestione
- Prognosi
- Screening
- Immagine 01
- Immagine 02
- Immagine 03
- Immagine 04
- Immagine 05
Insulinoma
Definizione e caratteristiche
- L’insulinoma è un raro tumore neuroendocrino pancreatico (definito anche pNET), che secerne insulina provocando una sindrome ipoglicemica.
- La maggior parte degli insulinomi è sporadica, tuttavia, circa il 5%-10% sono associati alla neoplasia endocrina multipla di tipo 1 (MEN1).
- Meno del 10% degli insulinomi assumo caratteri di malignità.
Localizzazione
- Più del 98% degli insulinomi sono localizzati nel pancreas, equamente distribuiti tra la testa, corpo e coda.
- Gli insulinomi localizzati al di fuori del pancreas sono estremamente rari (riportati in < 2% dei casi), e più frequentemente riscontrati nella mucosa duodenale, nei dotti biliari, nel diverticolo di Meckel, nell’ovaio e nell’omento.
Varianti
- pNET secernenti:
- il gastrinoma e l’insulinoma sono i più comuni;
- tra i tumori meno comuni vengono inclusi:
- glucagonoma;
- somatostatinoma;
- VIPoma (rilascia peptide intestinale vasoattivo);
- GRHoma (produce il peptide di rilascio dell’ormone della crescita);
- ACTHoma (produce l’ormone adrenocorticotropo, raro);
- PTHrp-oma (rilascia il peptide correlato all’ormone paratiroideo, raro);
- pNETs che causano la sindrome da carcinoide (rari).
- pNET non secernenti:
- questi tumori non producono sintomi specifici;
- possono secernere peptidi come:
- polipeptide pancreatico;
- cromogranina A;
- enolasi neurone-specifica;
- subunità della gonadotropina corionica umana;
- calcitonina;
- neurotensina.
Epidemiologia
Popolazioni a rischio
- Riscontrato con maggiore frequenza tra la terza e la quinta decade, con picco di incidenza tra i 40-45 anni.
- Circa il 60% dei casi sono riscontrati in pazienti di sesso femminile.
- Gli insulinomi associati alla MEN 1 sono tipicamente diagnosticati in età più precoce (29-34 anni).
- Circa il 50% dei pazienti affetti da MEN 1 presenta tumori neuroendocrini pancreatici, compreso l’insulinoma.
Eziologia e patogenesi
Cause
- Gli insulinomi sono prevalentemente sporadici, ma possono associarsi a sindromi genetiche (MEN 1)
- Solitamente, la MEN 1 è dovuta a fenomeni di eredità autosomica dominante della mutazione nel gene soppressore del tumore MEN1, e, meno comunemente, ad una mutazione de novo in MEN1.
| Caratteristiche del tumore | Sporadico | Associato a MEN 1 |
| Frequenza | 90-95% degli insulinomi | 5-10% |
| Numero delle lesioni | 1 | Variabile, solitamente multiple |
| Dimensioni | < 2cm | < 2cm |
| Potenziale di malignità | Basso | Basso |
Tabella 1. Insulinomi sporadici ed associati a MEN 1. MEN 1, neoplasia endocrina multipla di tipo 1.
Patogenesi
- Gli insulinomi hanno origine dalle cellule neuroendocrine o dalle cellule staminali multipotenti del pancreas e sono in grado di secernere insulina indipendentemente dai livelli ematici di glucosio:
- l’insulina induce un calo della glicemia inibendo la glicogenolisi, la gluconeogenesi, la lipolisi e la chetogenesi;
- basse concentrazioni ematiche di glucosio portano allo sviluppo di un’ipoglicemia iperinsulinemica, che si verifica a causa della mancanza di fonti alternative di energia;
- i sintomi si sviluppano a seguito dell’alterazione metabolica nel sistema nervoso centrale, con effetto riflesso anche sul sistema orto e parasimpatico.
- Nonostante la maggior parte degli insulinomi sporadici siano idiopatici, mutazioni somatiche del gene YY13 sono state riscontrate in alcune neoplasie insorte de novo.
- Patogenesi degli insulinomi associati alla MEN 1:
- il gene MEN1 codifica per la proteina menina, una proteina nucleare coinvolta nella regolazione della trascrizione, mantenimento della stabilità del genoma, divisione cellulare e proliferazione:
- se entrambi gli alleli MEN1 vengono inattivati, la proteina perde la sua funzione di soppressore tumorale, con conseguente sviluppo dei tumori associati a MEN 1;
- la compresenza di mutazioni ereditate o de novo nel gene MEN1, e di una mutazione somatica acquisita (una mutazione puntiforme o più comunemente una delezione) provoca la perdita di eterozigosi e la crescita clonale.
- il gene MEN1 codifica per la proteina menina, una proteina nucleare coinvolta nella regolazione della trascrizione, mantenimento della stabilità del genoma, divisione cellulare e proliferazione:
Storia e caratteristiche cliniche
Presentazione clinica
- Gli insulinomi sono tipicamente di piccole dimensioni e i sintomi sono solitamente associati all’ipoglicemia piuttosto che all’effetto massa.
- I sintomi possono essere aspecifici, portando a conseguenti ritardi nella diagnosi:
- l’ipoglicemia si presenta tipicamente a digiuno o dopo l’esercizio fisico, ma può anche svilupparsi indipendentemente dallo stato metabolico del soggetto;
- nelle fasi iniziali della malattia, i sintomi possono essere intermittenti, rispecchiando quella che è la secrezione pulsatile di insulina da parte del tumore, ma col tempo possono divenire persistenti;
- la gravità della sintomatologia non è correlata alle dimensioni del tumore o alla malignità.
- Nei pazienti con insulinomi può essere presente la triade patognomica di Whipple:
- segni e sintomi suggestivi di ipoglicemia;
- livello di glucosio plasmatico < 54 mg/dL (3 mmol/L) misurato durante la crisi ipoglicemica;
- risoluzione dei sintomi dopo la somministrazione di glucosio.
- I segni e i sintomi dell’ipoglicemia possono rimanere subclinici finché i livelli di glucosio nel plasma non raggiungono concentrazioni ≤ 50 mg/dL (2,8 mmol/L):
- tra i segni e sintomi neuroglicopenici si ritrovano:
- cefalea;
- vertigini/stordimento;
- diplopia o visione offuscata;
- sonnolenza/letargia e difficoltà di risveglio;
- irritabilità;
- stato mentale alterato e comportamento improprio;
- amnesia, confusione;
- debolezza;
- disartria;
- parestesie;
- convulsioni;
- coma.
- la sintomatologia autonomica causata dall’iperattivazione dei sistemi adrenergico e colinergico, si verifica a concentrazioni di glucosio < 60 mg/dL (3,3 mmol/L):
- segni e sintomi adrenergici possono includere:
- palpitazioni;
- tachicardia;
- tremori;
- pallore;
- ansia;
- nausea.
- i segni e i sintomi colinergici possono includere:
- sudorazione;
- senso di fame;
- sensazione di calore.
- segni e sintomi adrenergici possono includere:
- tra i segni e sintomi neuroglicopenici si ritrovano:
Anamnesi
- Indagare sulle caratteristiche dei sintomi, la durata, i fattori precipitanti (come il digiuno o l’esercizio fisico) e i fattori allevianti (come il consumo di cibo/carboidrati).
- Chiedere della storia personale o familiare di:
- qualsiasi endocrinopatia, in particolare di iperparatiroidismo o di adenomi ipofisari, che sarebbero suggestivi di insulinoma associato a MEN 1;
- gastrinoma o altri rari tumori neuroendocrini funzionanti del pancreas;
- tumori neuroendocrini pancreatici non secernenti.
Esame obiettivo
- Esaminare i segni di ipoglicemia.
- Analizzare l’aumento ponderale dovuto al consumo compensatorio di carboidrati per evitare l’ipoglicemia.
Diagnosi
- La diagnosi di iperinsulinismo endogeno viene effettuata sulla base dei seguenti criteri:
- livelli di glucosio ematico < 55 mg/dL (3 mmol/L);
- livelli di insulina ≥ 3 microunità/mL (18 pmol/L), durante la crisi ipoglicemica;
- livelli di C-peptide ≥ 0,6 ng/mL (0,2 nmol/L);
- livelli di proinsulina ≥ 5 pmol/L;
- mancanza di sulfonilurea nel plasma e/o nelle urine;
- livelli di beta-idrossibutirrato ≤ 2,7 mmol/L:
- raramente, alcuni pazienti con insulinoma possono avere livelli di beta-idrossibutirrato > 2,7 mmol/L, soprattutto se hanno avuto una precedente pancreasectomia parziale e devono essere perciò valutati per eventuali recidive.
- Sospettare un insulinoma in pazienti senza cause apparenti di ipoglicemia, come l’uso di insulina e sulfaniluree.
- Nei pazienti che presentano la triade di Whipple, il gold standard per la diagnosi di insulinoma è il test del digiuno di 72 ore (capacità diagnostica > 95%):
- dosare la glicemia ogni 6 ore fino a quando i livelli sono < 59 mg/dL (3,27 mmol/L), poi controllare ogni 2 ore per tutta la durata del digiuno;
- oltre a misurare il glucosio plasmatico, valutare:
- insulina;
- C-peptide;
- proinsulina;
- beta-idrossibutirrato.
- il test è considerato positivo quando si verifica uno dei seguenti eventi:
- livelli di glucosio ematico < 45 mg/dL (2,5 mmol/L) con segni o sintomi di ipoglicemia;
- livelli di glucosio ematico < 54 mg/dL (3 mmol/L) senza segni o sintomi di ipoglicemia con triade di Whipple precedentemente documentata.
- terminare il digiuno senza segni o sintomi di ipoglicemia depone per un test negativo.
- La localizzazione del tumore può essere confermata con studi di imaging, quali la tomografia computerizzata (TC) e/o l’ecografia endoscopica.
- Indice della malignità dell’insulinoma non è rappresentato dalle caratteristiche istologiche del tumore, bensì dall’evidenza di invasione degli organi circostanti o dalla presenza di metastasi.
Panoramica dei test
- Gli esami ematici sono necessari per confermare una diagnosi di iperinsulinemia endogena inappropriata (come quella dovuta all’insulinoma) in pazienti con segni e sintomi di ipoglicemia.
- Studi di imaging preoperatorio dovrebbero essere eseguiti per localizzare il tumore all’interno del pancreas:
- le tecniche non invasive rappresentano esami di prima linea:
- la TC trifase con contrasto dell’addome rappresenta il metodo di imaging più comunemente utilizzato;
- la risonanza magnetica (RM) (meno frequentemente disponibile della TC ma in grado di rilevare tumori più piccoli);
- l’ecografia transaddominale (ampiamente disponibile ma meno sensibile della TC o della RM).
- l’ecografia endoscopica (EUS) rappresenta l‘indagine associata alla massima accuratezza diagnostica per gli insulinomi e può essere utilizzata se i risultati ottenuti con le tecniche meno invasive non sono definitivi;
- altre tecniche di imaging meno comunemente utilizate per localizzare l’insulinoma includono:
- la tomografia ad emissione di fotone singolo (SPECT) del recettore della somatostatina e la tomografia ad emissione di positroni (PET);
- SPECT/PET del recettore del glucagon-like peptide-1 (Exendin-4);
- 18F-DOPA PET;
- l’ecografia intraoperatoria;
- la scintigrafia al 68-gadolinio.
- il test della stimolazione selettiva del calcio arterioso (SACST) presenta un’alta sensibilità, ma, a causa della sua natura altamente invasiva, è riservato a situazioni in cui altri test, incluso l’EUS, non riescono a visualizzare una lesione.
- le tecniche non invasive rappresentano esami di prima linea:
- La biopsia endoscopica con ago aspirato (FNA) guidata da ultrasuoni può essere eseguita in pazienti selezionati con sospetto di insulinoma e risultati non definitivi al test del digiuno e/o agli studi di imaging.
Stadiazione
- Stadiazione dell’American Joint Committee on Cancer (AJCC) per i tumori neuroendocrini del pancreas, ottava edizione:
- definizioni delle abbreviazioni di stadiazione:
- tumore primario (T):
- TX – il tumore primario non può essere valutato;
- T1 – tumore limitato al pancreas (nessuna invasione di organi adiacenti [stomaco, milza, colon, ghiandola surrenale] o parete di grandi vasi [tripode celiaco o arteria mesenterica superiore]; l’estensione del tumore nel tessuto adiposo peripancreatico non è rilevante ai fini della stadiazione) e dimensioni < 2 cm;
- T2 – tumore limitato al pancreas e di dimensioni comprese tra i 2 e i 4 cm;
- T3 – tumore limitato al pancreas e dimensioni > 4 cm, o tumore che invade il duodeno o il dotto biliare;
- T4 – tumore che invade organi adiacenti (stomaco, milza, colon, ghiandola surrenale) o parete di grandi vasi (tripode celiaco o arteria mesenterica superiore);
- per tumori multipli:
- aggiungere (m) per indicare tumori multipli;
- riferirsi al tumore più grande per l’assegnazione della T.
- linfonodi regionali (N):
- NX – i linfonodi regionali non possono essere valutati;
- N0 – nessun coinvolgimento linfonodale regionale;
- N1 – coinvolgimento dei linfonodi regionali.
- metastasi a distanza (M):
- M0 – nessuna metastasi a distanza;
- M1 – metastasi a distanza:
- M1a – metastasi confinate al fegato;
- M1b – metastasi in ≥ 1 sito extraepatico, come polmone, ovaio, linfonodo non regionale, peritoneo e osso;
- M1c – metastasi sia epatiche che extraepatiche.
- tumore primario (T):
- definizioni delle abbreviazioni di stadiazione:
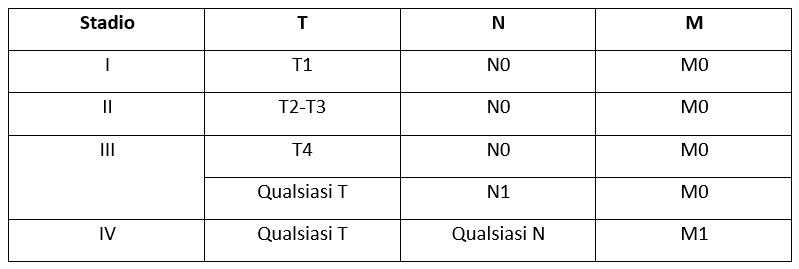
Tabella 2. Stadiazione.
Gestione
- Si rendono necessari aggiustamenti dietetici per prevenire l’ipoglicemia associata a periodi prolungati di digiuno in pazienti con insulinoma:
- piccoli pasti frequenti nel corso della giornata e in momenti critici come la sera tardi (prima di andare a letto) e la mattina presto;
- consumare carboidrati a lento assorbimento, come gli amidi complessi, il pane integrale, le patate con la buccia e il riso integrale;
- durante gli episodi ipoglicemici, assumere carboidrati a rapido assorbimento, come i succhi di frutta con l’aggiunta di ulteriore glucosio o saccarosio se necessario per garantire un rapido ritorno alla normoglicemia.
- La chirurgia è l’unico trattamento potenzialmente curativo per i pazienti con insulinoma, ed è raccomandata in tutti i casi in cui il tumore può essere localizzato e che non si presentano controindicazioni alla chirurgia:
- le controindicazioni possono includere gravi comorbidità, alto rischio anestesiologico, età avanzata o malattia ricorrente non resecabile dopo un primo intervento;
- la chirurgia può essere eseguita con tecniche laparoscopiche o a cielo aperto:
- la chirurgia laparoscopica è preferita nei pazienti con un singolo insulinoma non maligno:
- nella maggior parte dei casi, l’enucleazione dell’insulinoma è sufficiente, tuttavia alcuni casi richiedono una resezione più estesa;
- tasso di successo nel 70%-100%.
- la chirurgia laparotomica è tipicamente utilizzata nei i pazienti con malignità o insulinoma associato alla MEN 1, a causa della maggiore probabilità di presentare tumori multipli:
- durante l’intervento, il pancreas può essere esaminato completamente e palpato bi-digitalmente, permettendo di localizzare fino al 70% degli insulinomi;
- i segni associati con la malignità da ricercare durante l’esplorazione chirurgica includono aumento focale della consistenza, infiltrazione del tessuto circostante, e/o dilatazione del dotto pancreatico.
- la chirurgia laparoscopica è preferita nei pazienti con un singolo insulinoma non maligno:
- La terapia farmacologica è spesso necessaria per controllare i sintomi dell’ipoglicemia, la crescita del tumore prima della chirurgia, la malattia metastatica e nei pazienti che non sono eleggibili per la chirurgia:
- il diazossido è un analogo non diuretico della benzotiazide, spesso usato nei pazienti con insulinoma per controllare i livelli ematici di glucosio e i sintomi dell’ipoglicemia:
- la dose più comunemente utilizzata è di 50-300 mg/die per os, che può essere aumentata fino a 600 mg/die;
- nei pazienti con insulinoma maligno, possono essere utilizzate dosi più elevate se tollerate;
- gli effetti avversi includono edema (in particolare se somministrato a dosi elevate), aumento di peso, nausea, insufficienza renale e irsutismo;
- nei pazienti che assumono diazossido si può rendere necessaria l’aggiunta di un diuretico (come l’idroclorotiazide) per gestire l’edema e la ritenzione di sodio.
- gli analoghi della somatostatina (SSA) vengono utilizzati per la loro capacità di sopprimere la secrezione di insulina, tuttavia, possono anche causare la riduzione del rilascio di glucagone attraverso l’attivazione del recettore della somatostatina 2 (SSTR):
- trattamento di prima linea nei pazienti con insulinoma maligno (a causa del loro effetto antiproliferativo);
- trattamento di seconda linea in pazienti con insulinoma e sintomi ipoglicemici refrattari al diazossido.
- il diazossido è un analogo non diuretico della benzotiazide, spesso usato nei pazienti con insulinoma per controllare i livelli ematici di glucosio e i sintomi dell’ipoglicemia:
- Considerazioni aggiuntive per la gestione della malattia metastatica:
- nei pazienti con insulinoma maligno, la chirurgia è raramente curativa e la gestione spesso richiede farmaci antiormonali e antitumorali a lungo termine per il controllo dei sintomi e della crescita tumorale;
- la chemioterapia, in aggiunta alle altre terapie, è indicata nei pazienti con insulinoma maligno, soprattutto quelli ad alto grado;
- la chemioterapia a bersaglio molecolare (everolimus o sunitinib) può essere utilizzata in pazienti con insulinoma metastatico inoperabile, refrattario alla chemioterapia tradizionale, o come alternativa alle terapie locoregionali;
- la terapia con radionuclidi dei recettori peptidici (PRRT) è stata utilizzata per i tumori neuroendocrini gastroenteropancreatici metastatici, compresi quelli con metastasi a distanza, e può aiutare a controllare l’ipoglicemia in alcuni pazienti con insulinoma.
Prognosi
- La maggior parte degli insulinomi (> 90%) sono benigni:
- il 77%-100% dei pazienti con insulinoma benigno vengono trattati con la chirurgia a scopo curativo;
- la sopravvivenza globale dopo la resezione chirurgica risulta del:
- 97% a 5 anni;
- 88% a 10 anni.
- < 10% degli insulinomi presentano caratteri di malignità.
- I fattori associati a una maggiore probabilità di malignità e a una minore sopravvivenza includono:
- dimensione del tumore ≥ 2 cm;
- Ki-67 > 2%;
- alcune caratteristiche molecolari, come:
- instabilità cromosomica;
- perdita cromosomica di 3p o 6q;
- guadagno cromosomico su 7q, 12q o 14q.
- Livelli di insulina sensibilmente elevati durante il test del digiuno sono associati a tumori di dimensioni notevoli e ad elevato indice Ki-67.
- Recidiva:
- se presente, compare solitamente entro 2,5-3 anni dalla resezione chirurgica;
- è più comune nei pazienti con tumori associati alla MEN 1
Screening
- Lo screening annuale con test biochimici è indicato nei pazienti con MEN 1:
- questo si compone di vari test:
- dosaggio del glucosio a digiuno a partire dall’età di 5 anni;
- dosaggio dell’insulina a digiuno a partire dai 5 anni di età.
- questo si compone di vari test:
Immagine 01
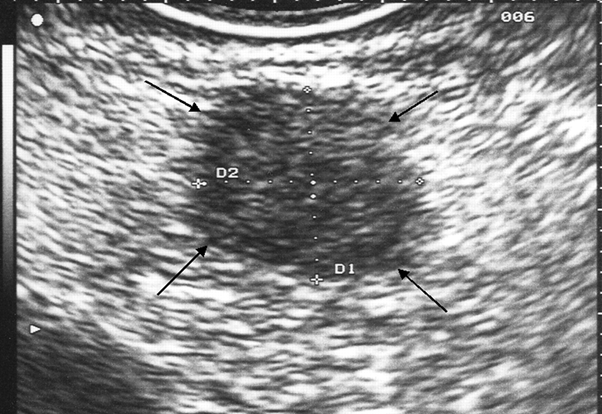
Immagine 01. Ecografia endoscopica preoperatoria in una paziente di 67 anni. Evidente il tipico aspetto ipoecogeno dell’insulinoma.
Immagine 02

Immagine 02. Sezione assiale di tomografia assiale computerizzata, che dimostra una lesione solida iperdensa localizzata nella testa del pancreas.
Immagine 03
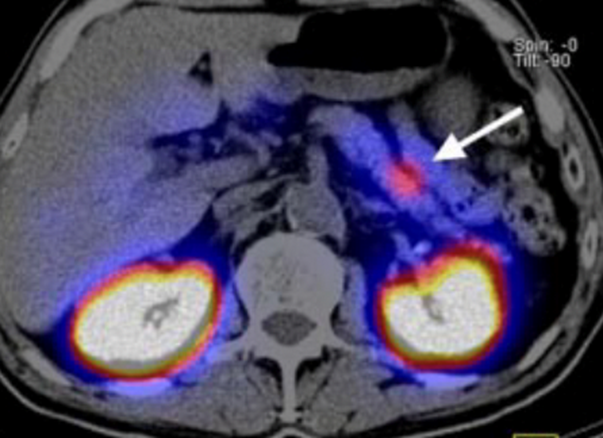
Immagine 03. SPECT scan a 6 giorni dopo la somministrazione del marcatore per la ricerca del recettore glucagon-like peptide 1 (Exendina 4). Nell’immagine si osserva una marcata captazione di tracciante a livello della coda del pancreas. La diagnosi è quella di insulinoma maligno.
Immagine 04
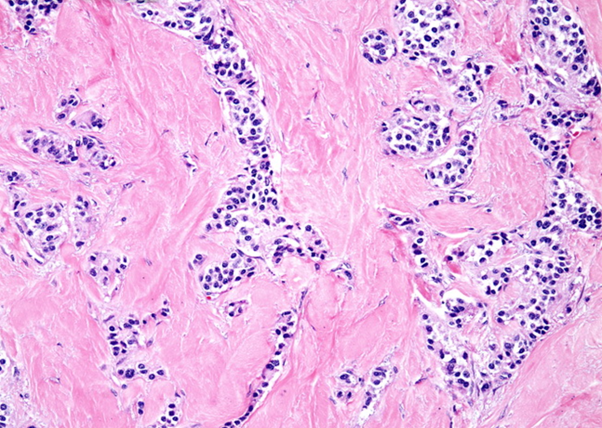
Immagine 04. Immagine microscopica di insulinoma secernente. Non esistono differenze istologiche che permettono di differenziare pNET secernenti da quelli non secernenti: in entrambi i casi si riscontrano architetture trabecolari, tubulo-acinari e solide.
Immagine 05
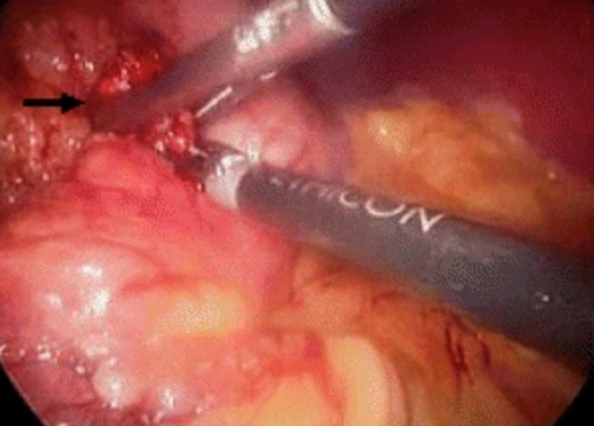
Immagine 05. Vista endoscopica di un insulinoma del corpo del pancreas, durante la sua enucleazione.